がん遺伝子治療スキルス胃がん
【がん遺伝子治療】症例(19) 40代女性 スキルス胃がん 腹膜播種
2024.07.08
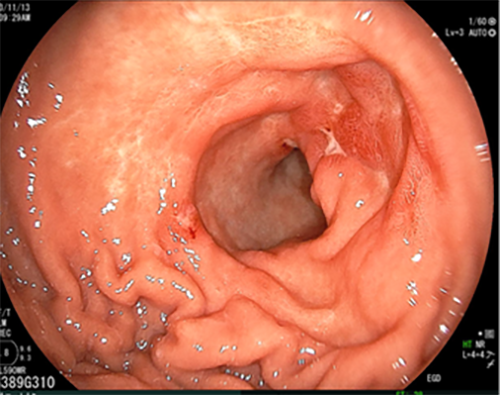
<治療開始2ヶ月後>
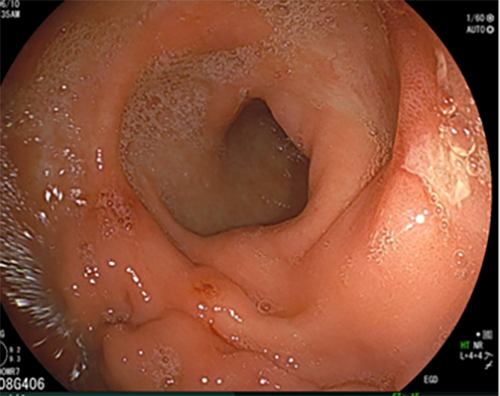
<治療開始9ヶ月後>
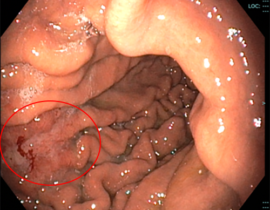
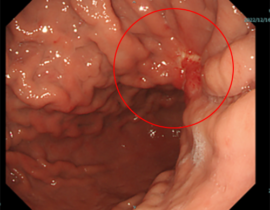
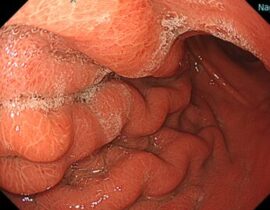
スキルス胃がん、腹膜播種、腸閉塞、胸水ありの状態で、遺伝子治療開始。2ヶ月で50億ベクターコピー数の遺伝子製剤を投与。治療開始後9ヶ月月経過し、胃病変の縮小、腹水減少が認められ、ほぼ症状は消失して日常生活に復帰している。
| ご相談内容 | 卵巣がんの診断で手術後、腹水発生し、 4型胃がん(スキルス胃がん)と診断されたが 標準治療だけでなく遺伝子治療を併用したい。 現在 腹水顕著 食思不振 腸閉塞気味 胸水もある。 |
|---|---|
| 治療方針 | 標準治療を補完する立場で、点滴、局所注射により遺伝子治療を実施。 |
| 治療経過 | 2023年8月 標準治療を行う医療機関で化学療法を開始。 標準治療でご本人入院のため、ご家族が遺伝子治療オンラインカウンセリング。 通院可能となったら、遺伝子治療は提供可能とお伝えする。 ご家族より「入院での抗がん剤治療が終わり、 通院に切り替わったので腹腔内化学療法と合わせて 遺伝子治療も始めたいと思っています。」と連絡あり、遺伝子治療を開始。 2023年9月 遺伝子製剤 10U(単位)投与。遺伝子治療の副作用はない。 初回10U 1~2週間間隔で 10~20U 1~2ヶ月で100~200U以上の送達を目指す。 標準治療を主軸とし、それに支障がないよう様に治療プランを立てる。 送達経路は ①点滴 ②腹腔内 の予定。 標準治療開始時は、イレウス(腸閉塞)状態。 CART後は経口摂取が可能になった。 今後パクリタキセル腹腔内投与とFolfox併用する予定。 「腹水を抜いてもらい、腹部膨満感もなくなり楽になった。 体重減少し体力の低下はある。 食欲もあるので経口摂取の許可が出てからはちょこちょこ食べています。」 「自分としては遺伝子治療に期待しているが、 しっかりと治療に取り組んでくださっている 標準治療担当医にどう説明すればよいでしょうか。」とのこと 早速当院より担当医師に説明。 2023年10月 遺伝子製剤 10Uを3回投与。 化学療法の副作用でだるさと胸やけ、 ガスが溜まっている感じがある。食欲はある。 10月上旬投与後、夕方より39℃の発熱あり。 解熱剤で翌日には平熱になった。 10月中旬投与後も発熱あり。解熱剤で下がるが、 薬効が切れるとまた上がり3日くらい続いた。 腹水貯留している様子や体調変化が無ければ、以降エコーなしで投与。 10月下旬投与後も発熱あったが、1日だけでおさまった。 2023年11月 遺伝子製剤 10Uを2回投与。 11月上旬に当院でEGD(上部消化管内視鏡検査)実施。 type4胃がん。前医での内視鏡imageと比較すると、胃の拡張は改善している。 Scope反転しての観察も可能。giant foldは変わらずあり。 「投与後に解熱剤を飲んだので熱は出ませんでした。 標準治療継続中。特に著変は無いが、腹部の張り感はやや気になる。 想定内と説明を受けているが診てもらいたい。」とのこと、 局注時エコーで腹水確認。 2023年12月 遺伝子製剤 10U投与。 体調特に変わりなし。 2024年1月 遺伝子製剤 10Uを2回投与。 「12月下旬のCTで、胃壁の厚さは改善していると標準治療担当医から言われた。 摂食、排泄は問題ない。 食欲もあるし、気になるのは腹水です。」 「1月の標準治療時にも腹水を抜いてもらった。 血液検査は問題なく炎症反応も落ち着いていて、 CA125(婦人科系腫瘍マーカー)も良かった。」 遺伝子治療の投与間隔は最大6週間あけて可。 2024年2月 遺伝子製剤 10U投与。 特に気になる症状なし。 2024年3月 遺伝子製剤 10U投与。 「体調は落ち着いています。 抗がん剤の副作用のことを考えると精神的にしんどいですね。 腹水中の細胞の検査も陰性でした。」 2024年4月 遺伝子製剤 5U投与。 遺伝子治療今回から5U1か月毎にtaperする。 「腹水貯留は変化なし。食事・排泄は良好。 4月に腹水細胞診実施したががん陰性、乳び認めず。 FolfoxはTaperか。化学療法後、腹部張り感はある。」 と標準治療担当医コメントあり。 「今は体調は悪くないです。抗がん剤の治療を受けた後はきついですが。 お腹のはりは慣れてきちゃったのかもしれませんが、 前よりそこまで張っていないと思います。」 2024年6月 遺伝子製剤 5U投与。 同日当院でEGD(上部消化管内視鏡検査)実施。 type4胃がん化学療法中。前回と比較して著変なし。 若干縮小しているようにも見える。 2024年7月 遺伝子製剤 5U投与。 「腹水細胞診は陰性だった。腹水は増量しなくなっている。」 7月の抗がん剤治療の後、腸閉そくと帯状疱疹で1週間入院。 2024年8月 遺伝子製剤 5U投与。 本人としては元気で食事排泄問題ない。 遺伝子治療を継続中。 ※2024/9追記 |
| 治療状況 | スキルス胃癌、腹膜播種による腸閉塞を発症し、腹部が大きく膨隆して摂食や排便が全くできない状態(予後が極めて不良と予測された状態)から治療が開始されました。 当院と連携した医療機関で標準治療、当院において遺伝子治療を実施。 初期治療の段階から症状は改善傾向あり。 治療を継続したところ、腹水減少傾向が見られ、経口摂取不良と腸閉塞の状況は完全に解消しました。 その後、抗がん剤、遺伝子治療の投与量いずれも減少傾向。 初期治療から約1年経過した現在、 元気で普通の生活をしており、癌細胞が消失している(確認されていない)のは奇跡的な経過と言えます。 |
| 治療期間 | 2023年9月~2024年8月(11か月)継続中 |
| 費用 | 治療費総額:計15回の治療で 計 6,292,000円。(税込) ※遺伝子製剤の投与量単位(U:unit)について:遺伝子治療製剤の投与ボリュームを表現する際に『Titer(遺伝子を運ぶウイルスベクター粒子の数または感染価)』『ベクターコピー数』 などが用いられます。投与量単位(U)は、当院で便宜上設定したもので公的な基準ではありません。具体的には、当院で設定している1Uは1.0×10^8(10の8乗)=1億ベクターコピーに相当します。 |
| 治療のリスク | 大規模な二重盲検試験が実施されておらず未承認治療です。 注射部の内出血、軽度疼痛、一過性の発熱(37℃超)など、軽微な副作用がある場合があります。 |