加齢に伴う身体的および生理的機能の低下(老化)に対する再生医療
【自家脂肪由来 間葉系幹細胞(MSC)治療】
「老化」は様々な疾患の原因になる
加齢に伴う身体的および生理的機能の低下、すなわち老化は、脳神経、心血管系、呼吸器系、消化器系、腎臓・泌尿器系、骨、筋肉、免疫系、視覚、聴覚、皮膚、精神的な側面など、さまざまな領域で現れます。この過程で発生する機能の低下は、ほとんどの場合、体にとって有害です。 厚生労働省の「介護が必要となった主な原因」の最新版(出典:厚生労働省2022年国民生活基礎調査より)によると、65歳以上の要介護者が介護を必要とする主な原因は、「認知症」「脳血管疾患(脳卒中)」「高齢による衰弱(フレイル)」「骨折や転倒」「関節疾患(変形性関節症など)」が上位に挙げられています。これらはまさに老化によって引き起こされる代表的な疾患群であり、生活習慣の見直しや、適切な医療介入を行うことでその進行を防ぐことが求められます。

出典:厚生労働省2022年国民生活基礎調査より
医療技術の進歩や生活環境の改善によって人々の寿命は延び、高齢化が進んでいますが、その結果、老化による疾患や障害によって介護を必要とする人々が増加しています。これが、高齢者を支える世代にも大きな負担を与え、全世代にわたる生活の質を損ない、社会全体の活力を低下させる原因となっています。老化現象をコントロールし、ただ長生きするのではなく、健康的に長生きできる社会を実現することは、個人や社会全体の幸福にとって非常に重要な課題です。 北青山D.CLINICでは、再生医療を、健康的な老化<Your Best Aging>医療プログラムの一環としても位置付けをし、適用疾患を取得し提供しています。
主な症状:ロコモ、フレイル、サルコペニア、光老化、がんなど
加齢による老化は様々な身体生理機能低下(老化)を引き起こし、老化が主因となる疾患は数多く存在します。心臓や脳などの主要臓器の機能に関わる血管病、骨・筋肉・関節などの劣化が原因となるロコモティブシンドローム・サルコペニア・フレイル、光老化が主因となる皮膚・皮下組織の劣化、ひいては悪性新生物(癌)の発生など、言うまでもなく老化は心身の恒常性(ホメオスタシス)の破綻による生命機能全般を悪化させます。
老化の代表的な概念である「ロコモティブシンドローム(ロコモ)」は加齢に伴う運動機能の低下を指す言葉です。また、高齢者の筋力低下によって身体機能が衰え、さらに抑うつや認知機能の低下により社会生活が困難になる「フレイル(虚弱)」という現象も、介護が必要な状態に至る点で注目されています。これらのロコモやフレイルは、骨や筋肉の老化による機能低下が引き起こす問題であり、ロコモが進行すると最終的にはフレイルに至ると言えます。
加えて、筋肉量が減少する「サルコペニア」という概念も1990年頃から老化現象を象徴する表現としてよく使われ、特に筋力と筋肉量の著しい減少を指します。ロコモ、フレイル、サルコペニアは、加齢による骨や筋肉の衰えに関する異なる側面を示しています。
これらの状態が進行することで、健康で快適な生活が送れなくなるばかりか、社会的な関わりも失われ、要介護状態に陥る人が増加しているため、これらの問題への関心が高まっています。老化の進行を抑えることは、ロコモ、フレイル、サルコペニアを予防することに繋がると言えるでしょう。
診断方法
老化の診断方法は多岐にわたりますが、基本的には身体的・認知的・生理的な変化を評価することで行われます。老化の診断には、個別の疾患や障害が原因となっている場合もあるため、総合的なアプローチが求められます。加齢現象に影響を与える要因として、環境要因、ホルモン変化、活性酸素ダメージ、遺伝子などが挙げられます。
- 身体的健康の評価
(1)身体検査:
筋力、関節の可動域、姿勢、歩行の速度や安定性などの評価
(2)血液検査:
ホルモンレベル(成長ホルモン、性ホルモンなど)、ビタミン・ミネラルの状態、血糖値や脂質などの代謝異常の調査
(3)心臓・血管の評価:
血圧や動脈硬化など、老化に伴う心血管の問題をチェックするため、血圧測定や動脈硬化度測定(CAVI検査)、頸動脈エコー検査などを行います。
- 認知機能の評価
(1)認知機能テスト:
例えば、ミニメンタルステート検査(MMSE)や時計描画テストなどが使われ、記憶力や注意力、言語能力、判断力などを測定します。
(2)MCI検査:
「アミロイドβペプチド」を脳内から排出したり、そのシナプスへの攻撃から防御したりする働きを持つ3種類のタンパク質(APOA1、TTR、C3)の血中濃度を調べ、その測定値から、統計学的手法により認知機能障害の程度を推定するものです。
(4)脳ドック(AI併用):
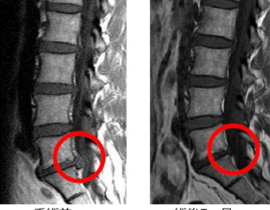
脳卒中(脳梗塞、脳出血、くも膜下出血)予防や脳腫瘍早期発見を意図した脳ドックにプラスして、 AIによる脳MRI画像(特に記憶中枢である海馬周囲)の解析と認知心理CQテストにより認知機能を厳密に評価します。
- 生理的変化の評価
(1)骨密度検査:
骨密度を測定することで、骨粗鬆症や骨折のリスクを評価します。
(2)視力・聴力検査:
視力や聴力の低下も老化の一環として進行することがあります。
(5)尿検査や便検査:
老化に伴い、消化器系や泌尿器系の健康状態も変化することがあります。
- 筋力と運動能力の評価
(1)歩行速度テスト:
歩行速度の低下は老化のサインとして重要であり、疾患のリスク評価にもつながります。
(2)握力測定:
握力は全身の筋力の指標としてよく使われます。握力が低下していると、身体の機能全般が低下している可能性があります。
- 生活の質(QOL)の評価
老化に伴い、生活の質(QOL)が低下することがあります。QOLを評価して老化度を診断することがあります。
- <テロメア検査>
老化の進行や疾患リスクに関与する遺伝的要因を調べるために、テロメア検査が行われることもあります。テロメアの状態が老化に関連していることが分かっており、早期に老化のリスクを把握するために有用です。
化学的診断(ドック・検査)について
化学的な老化の診断として当院では「エイジングケアドック」や「テロメア」検査、「MCI検査」「リキッドバイオプシー」を行っています。<エイジングケアドック>
エイジングケアドックは、血管年齢、肺年齢、骨年齢、ホルモン年齢、酸化障害度、免疫年齢などを測定し、老化度(加齢度)を客観的に評価するものです。【検査項目】
<テロメア検査>
テロメアは、染色体の端に存在する構造で、染色体内の重要な遺伝情報を保護しています。この構造は細胞の老化に深く関わっており、加齢に伴うさまざまな疾患とも関連しています。テロメア検査では、テロメアの状態を分析し、個人の遺伝的な強さ(テロメア強度)や日々のストレスによる遺伝子の疲労度(テロメア疲労度)を測定します。<MCI検査>
アルツハイマー病の原因物質である「アミロイドβペプチド」は、脳内から脊髄液を介して血液に排出されます。「アミロイドβペプチド」は、脳内に蓄積し、神経細胞にダメージを与え、記憶や認知機能を担うシナプスを障害すると言われています。このMCI検査は、「アミロイドβペプチド」を脳内から排出したり、そのシナプスへの攻撃から防御したりする働きを持つ3 種類のタンパク質( APOA1、TTR、C3 )の血中濃度を調べます。その測定値から、統計学的手法により認知機能障害の程度を推定するものです。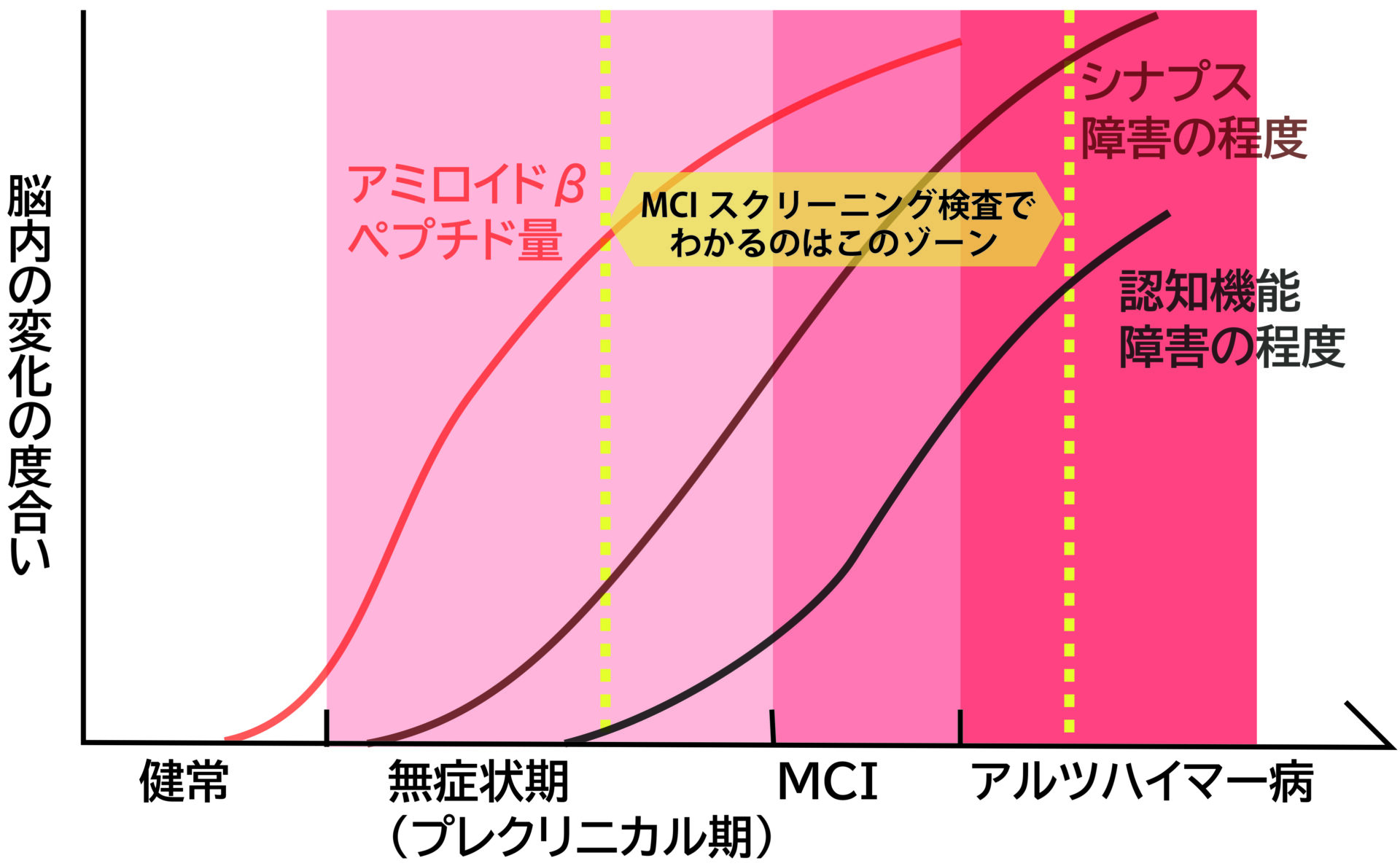
<リキッドバイオプシー>
リキッドバイオプシーとは血液、尿、唾液、脳脊髄液、心嚢膵、胸水、腹水、便などの体液サンプルを用いてゲノム解析を行う検査です。血液、尿、だ液などの採取だけなので、患者さんは少ない負担で検査を受けていただくことができます。当院ではリキッドバイオプシーをがんや認知症の早期発見、予防のためにご提供しています。予防
生命活動を維持する過程で加齢(aging)は避けられませんが、加齢に伴う身体的・生理的機能の低下、すなわち老化(senescence)は、適切な介入によりその進行を遅らせたり、防いだりすることが可能です。また、老化は多くの疾患の主な原因となるため、老化の進行を抑制することは、その関連疾患の予防にも繋がります。以下の方法を実践することで老化の進行を遅らせ、健康的な老化<Your Best Aging>につなげることが可能です。

出典:厚労省の推奨するフレイス予防3つのポイント
- バランスの取れた食事
抗酸化物質(ビタミンC、ビタミンE、ポリフェノール)を多く含む食品、オメガ3脂肪酸、タンパク質の摂取を心がけましょう。また、いくつかの研究では、カロリー制限が寿命を延ばし、老化を遅らせる可能性があることが示唆されています。
- 定期的な運動
歩行、ランニング、サイクリング、水泳などの有酸素運動は心肺機能を高め、血流を改善し、健康的な体重を維持するのに役立ちます。また、筋肉量の減少を防ぐために、週に数回の筋力トレーニングを行うことが推奨されます。ダンベルや自重トレーニングなどを取り入れましょう。ヨガやストレッチ、太極拳などは柔軟性を保ち、転倒のリスクを減らすことができます。 - 十分な睡眠
質の良い睡眠は老化を防ぐための基本です。睡眠中に成長ホルモンが分泌され、細胞の修復や再生が行われます。毎晩7~8時間の睡眠を規則正しく確保することが理想的です。睡眠不足や不規則な生活は老化を加速させる可能性があります。 - ストレス管理
慢性的なストレスは身体に悪影響を与え、老化を促進する原因となります。ヨガや瞑想を取り入れて、心身をリラックスさせる時間を持つことが効果的です。深呼吸やリラクゼーションテクニックもストレス軽減に有効です。また、趣味や好きなことに時間を使うことは心の健康を保ち、ストレスを軽減します。 - 社会的なつながり
社会的なつながりは、精神的な健康に重要であり、孤独を避けることが老化予防に役立ちます。定期的に家族や友人と会ったり、オンラインでのコミュニケーションを取り、孤立を避けることが大切です。ボランティア活動や地域活動に参加することも、社会とのつながりを持ち、充実感を得ることができます。 - 禁煙と適度な飲酒
喫煙や過度な飲酒は老化を加速させ、様々な健康問題を引き起こします。 - 健康診断と早期発見
定期的に健康診断を受けることは、老化に伴う病気や疾患の早期発見に繋がり、予防や早期治療が可能になります。血糖値やコレステロール、ホルモンの状態をチェックし、問題があれば早期に対処することが重要です。 - 積極的な学習と精神的刺激
新しいことを学んだり、社会的な対話に参加することで、思考を活発に保つことができます。
加齢に伴う身体的および生理的機能の低下と再生医療
再生医療は、間葉系幹細胞を活用することで、修復や再生能力を持つこれらの細胞を利用し、現代医療技術では治療が難しい疾患に対して有効な治療法として注目されています。しかし、再生医療は従来の治療法とは異なる成果を上げる可能性がある一方で、完全に万能な治療法ではなく、治療効果には限界があります。幹細胞の機能には個人差があり、さらに組織幹細胞には本来の限界が存在します。それでも、自身の修復・再生力を最大限に活用するため、倫理的な問題はなく、安全性も確認されているため、この治療法は非常に合理的な予防医療の一環として活用できます。
当院では再生医療の適応疾患として「加齢に伴う身体的および生理的機能の低下に対する再生医療」(および他の老化に関連する疾患「認知機能低下」「動脈硬化」「慢性疼痛」「運動器(骨・筋肉・関節・神経)障害」「慢性肺疾患」「慢性腎疾患」「動脈瘤」についても受理済)を厚生労働省に届け出を受理されており、老化に伴う諸症状の改善に関する治療実績があります。
①Ichihashi M, Tanaka M, Iizuka T, Nagoe N, Sato Y, et al. Therapeutic Effect of Intravenously Administered Autologous Adipocyte-Derived Stem Cells on Chronic Stage Stroke Patients. Int J Stem Cell Res Ther 2020; 7:070.
加齢は脳卒中発症の危険因子の1つであり、脳卒中は再発により重症化することが問題視される。すなわち脳卒中の管理においては一次予防 (発症予防)のみならず、二次予防 (再発予防) のための慢性期治療も重要である。 本研究では、脳卒中を発症した21名の患者を対象として自家脂肪由来間葉系幹細胞(ADSC)を投与し経過観察した。患者の発症時の年齢は40-79歳。ADSC投与後早期から運動、感覚、認知機能の回復、また皮膚温度の上昇が確認された。また、脳卒中神経学的重症度の評価スケール(NIHSS)での改善もADSC投与約2〜3時間後という早い段階で確認された。さらに、脳卒中発症後6ヶ月以内にADSCを投与された患者は、12ヶ月以降に治療を受けた患者と比較して機能回復がより顕著であった。
②Tsang KS, Ng CPS, Zhu XL, Wong GKC, Lu G, Ahuja AT, Wong KSL, Ng HK, Poon WS. Phase I/II randomized controlled trial of autologous bone marrow-derived mesenchymal stem cell therapy for chronic stroke. World J Stem Cells. 2017 Aug 26;9(8):133-143. 慢性脳卒中患者を対象とした自家骨髄由来間葉系幹細胞(MSC)の臨床試験(a randomized, controlled, double-blind, phase I/II clinical trial)。
年齢41~59歳の9人を2群に分け、5人に4週間隔で2回MSCを、4人にプラセボ群としてヒト由来アルブミンを投与した。結果として、プラセボを投与された患者と比較してMSCが投与された患者は神経回復と臨床的改善が明らかだった。この研究はMSCの静脈内投与が脳内出血の発症後重度障害を持つ患者の神経機能の回復を促すことを示唆した。
③Stavely R, Nurgali K. The emerging antioxidant paradigm of mesenchymal stem cell therapy. Stem Cells Transl Med. 2020; 9(9):985-1006.
加齢に伴う活性酸素の過剰産生が原因の酸化ストレスは、細胞障害、炎症、代謝異常をきたし、老化や様々な疾患の原因になることが知られている。本レビューでは、種々のin vivo及びin vitroモデルにおいて間葉系幹細胞(MSC)の抗酸化作用が確認された。様々な動物の疾患モデルにおいて、MSCは抗酸化物質を産出して細胞保護、抗炎症作用をもたらすこと、また、フリーラジカルの消去、内因性抗酸化力の増進、活性酸素種抑制に伴う免疫調節などによって細胞内のミトコンドリアの生物学的活性の改善に寄与することが示唆された。
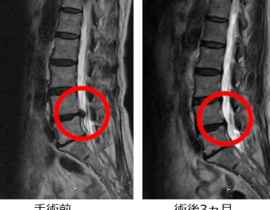
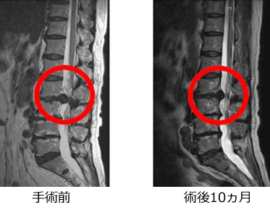
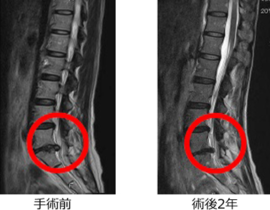
④JeongHyun Shim, Kyoung‐Tae Kim, Kwang Gi Kim, Un‐Yong Choi, Jae Won Kyung, Seil Sohn, Sang Heon Lim, Hyemin Choi, Tae‐Keun Ahn, Hye Jeong Choi, Dong‐Eun Shin, Inbo Han, Safety and efficacy of Wharton's jelly‐derived mesenchymal stem cells with teriparatide for osteoporotic vertebral fractures: A phase I/IIa study, 2020
骨粗鬆症性脊椎圧迫骨折患者を対象とした幹細胞MSCの最初の臨床試験(randomized, open‐label, phase I/IIa study)報告。年齢50~89歳の20人の患者を2群に分け、テリパラチド(human parathyroid hormone、PTH)及びウォートンゼリー由来の間葉系幹細胞(WJ-MSC)の併用治療とテリパラチド単体の治療を比較した。前者は、テリパラチド20μg/日を6か月間投与及びWJ-MSCの髄腔内投与(4×107個細胞)+静脈内投与(2×108個細胞)の併用、後者はテリパラチド20μg/日を6か月間投与とした。各群の7人に対して1年間の追跡調査を行ったところ、併用治療のグループにおいて痛みの緩和や骨密度の増加など良好な改善が見られた。
⑤Golpanian S, DiFede DL, Khan A et al. Allogeneic human mesenchymal stem cell infusions for aging frailty. J Gerontol A Biol Sci Med Sci. 2017; 72:1505–1512
加齢が原因のフレイル(虚弱)に対する他家骨髄由来間葉系幹細胞(MSC)投与の第I相非盲検試験の結果報告。 MSC は20〜45歳健常者の骨髄から収集された。平均年齢78歳の15名の虚弱患者を3群に分け、それぞれを5千万、1億及び2億個のMSCを単回静脈内注入した。治療後特に重篤な有害事象は見られず、6ヶ月後の追跡調査では、全群において6分間の歩行距離及び腫瘍壊死因子α(TNF-α)値が改善された。特に、1億個細胞投与群ではSF-36における身体機能評価の指標値が大幅に改善した。
⑥Tompkins B, Difede D et al. Allogeneic mesenchymal stem cells ameliorate aging frailty: a phase II randomized, double-blinded, placebo controlled clinical trial. J Gerontol A Biol Sci Med Sci. 2017; 72:1513–1521.
加齢が原因のフレイル(虚弱)に対する他家骨髄由来間葉系幹細胞(MSC)投与の第II相ランダム化二重盲検試験(上記⑤の続き)の結果報告。 平均年齢76歳の30人虚弱患者を3群分けた。1群(10人)に1億個MSC、2群(10人)に2億個MSC細胞、3群(10人)はプラセボを単回静脈内投与した。重篤な有害事象は発生しなかった。投与後6ヵ月で検査したところ、免疫学的改善は1群、2群共に観察されたが、身体能力の改善は1群において顕著だった。
⑦Jessica Hiu-tung Lo, Kin Pong U, Tszlam Yiu, Michael Tim-yun Ong, Wayne Yuk-wai Lee, Sarcopenia: Current treatments and new regenerative therapeutic approaches, Journal of Orthopaedic Translation, 2020; 23: 38-52,
加齢による筋肉量及び筋力の低下はサルコペニアと称され、その原因はミトコンドリアの機能障害と加齢に伴う筋肉炎症とされる。 最近の臨床研究レビューによると、サルコペニアの改善には、栄養補助食品や医薬品はあまり有効ではなく、身体運動が最も有効な方法である。運動は、ミトコンドリアの恒常性を回復させ、骨と筋肉間でのシグナル伝達物質を介した抗炎症反応を惹起することが示されている。一方、運動を導入できない高齢のサルコペニア患者に対しては、間葉系幹細胞(MSC)投与が有望な治療オプションとなる可能性がある。MSCがもつミトコンドリア機能回復効果と免疫調節能及びMSCから産生される抗炎症性サイトカインの効果によりサルコペニアの改善が期待できる。
⑧Charles-de-Sá, Luiz & Gontijo de Amorim, Natale Ferreira & Sbarbati, Andrea & Benati, Donatella & Bernardi, Paolo & Carias, Rosana & Rigotti, Gino. Photoaging Skin Therapy with PRP and ADSC: A Comparative Study. Stem Cells International. 2020. 1-13.
肌の光老化に対する脂肪由来間葉系幹細胞(ADMSC)移植に関する前向き無作為比較試験。年齢45~65歳の20人を二群に分け、自家PRPと自家ADSCを皮下投与、投与前と投与4ヶ月後の皮膚生検像を比較した。PRPは皮膚に炎症を惹起することによりコラーゲン線維を増やし真皮網状層を厚くするものの組織再生は見られなかったのに対し、ADSCは細胞外基質再構築、新たな弾性線維の増加などの皮膚の再生を認めた。
⑨Chen, S., He, Z. & Xu, J. Application of adipose-derived stem cells in photoaging: basic science and literature review. Stem Cell Res Ther .2020,11, 491
紫外線への継続的な曝露は皮膚老化を促進し、皮膚癌の発生リスクを増大させることは良く知られている。皮膚の光老化に対する脂肪由来幹細胞(ADSC)の治療効果を評価するための前臨床試験をレビューした。ADSC自体が有する増殖能や分化能に加えてADSCから分泌される種々の成長因子やサイトカインの効果が、紫外線による皮膚老化の改善、皮膚癌の治療に有益であると言える。
脂肪由来 間葉系幹細胞(mesenchymal stem cell: MSC)療法とは
身体の中には組織の修復効果を持つさまざまな幹細胞が存在しており、中でも骨髄や脂肪の中に潜む間葉系幹細胞は再生医療の素材として高く注目されています。特に脂肪由来の間葉系幹細胞は骨髄由来のものに比べて以下の優位点があることから研究や治療に広く用いられるようになっています。
- ・幹細胞を抽出できる脂肪細胞は、骨髄細胞に比較して容易にかつ低侵襲に採取できる
- ・脂肪由来 間葉系幹細胞は骨髄由来と同様の脂肪・骨・軟骨への分化能に加えて骨髄由来にはない筋分化能も持つことが示されている
- ・脂肪由来 間葉系幹細胞は、細胞形態や分化能は骨髄由来と差異はないが、増殖能が強く、増殖に伴う老化の影響や骨分化能の低下が少ない
この期待できる脂肪由来間葉系幹細胞を体内から取り出した少量の脂肪から分離し、特殊な環境下で大量に培養したものを、体内(患部)に注射や点滴で送達する治療法を、脂肪由来間 葉系幹細胞療法もしくは幹細胞移植と呼びます。
脂肪由来 間葉系幹細胞療法は、今まで有効な治療法がない様々な疾患に対して外来治療で対応できる点が高く評価されます。中でも加齢に伴う身体的および生理的機能の低下の改善への期待できる治療として国際的に盛んに実施されています。
薬理効果
脂肪由来 間葉系幹細胞は、加齢に伴う身体的および生理的機能の低下の改善に対して幹細胞移植による血管新生作用、パラクライン作用、免疫調節作用、抗炎症作用のいずれかにより治療効果が期待できることが示されています。
治療の流れ・費用・リスク
加齢に伴う身体的および生理的機能の低下(老化)に対する 脂肪由来 間葉系幹細胞による治療は具体的には以下のステップがあります。
- カウンセリング
- 問診・血液検査:
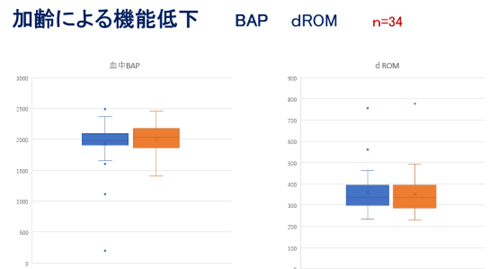
①血中dROM値 (酸化ダメージの指標値)の評価
②血中BAP値 (抗酸化力の指標値) の評価
- 脂肪切除: 腹部や膝裏など、3㎜程度の切開により米粒大数粒の脂肪を切除(局所麻酔で外来処置)
- 間葉系幹細胞分離培養: 切除した脂肪細胞から間葉系幹細胞を分離し細胞培養加工室で増殖培養(3-4週間)
- 間葉系幹細胞投与: 増殖培養した間葉系幹細胞1億個以上を、点滴投与により体内へ送達
- 経過観察
治療費用
治療費用はこちらから治療のリスク
採血時:穿刺部疼痛、皮下出血、神経障害 ・脂肪採取時:疼痛、感染、皮下出血、硬結、色素沈着 ・培養時:培養遅延、汚染 ・投与時:注射部痛、灼熱感、発熱、悪心、呼吸症状(血栓症) ・治療後:症状回復遅延、治療効果不足 ※但し、適切に治療を遂行すれば、重篤な有害事象が生じるリスクは極めて低いと言えます。「加齢による身体的生理的機能低下に対する脂肪由来間葉系幹細胞治療」の適応
治療適応は、加齢による身体的生理的機能低下の状態にあり、その改善や増悪予防を希望される方。 具体的には以下の病態や症候が治療対象になります。
- 加齢に伴う老化が原因となる身体生理機能の低下及び障害
- 脳卒中、心血管障害などの動脈硬化を背景にした疾患群
- 活性酸素、フリーラジカルに対する抵抗力の低下
- 活性酸素、フリーラジカルによる酸化障害の増加
- 皮膚の光老化
- 骨量低下
- 筋肉量ないしは筋力の低下(サルコペニア)
- 虚弱(フレイル)
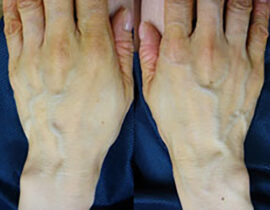
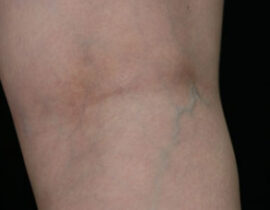
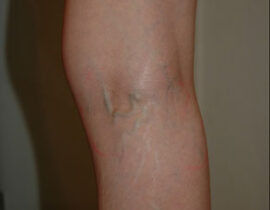
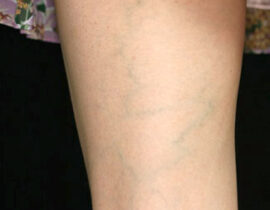
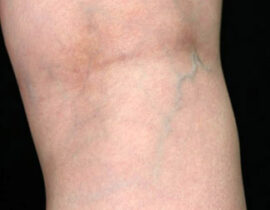
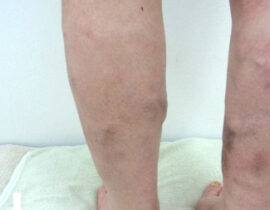
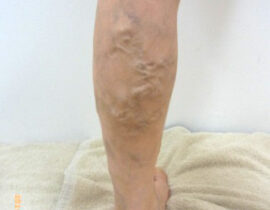
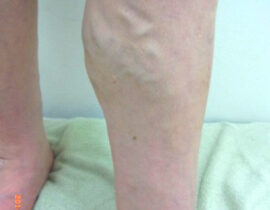
実際の症例
治療評価について
当院では、加齢に伴う身体的および生理的機能の低下に対する再生医療(幹細胞治療)治療を
- 血中BAP値 (抗酸化力の指標値)
- 血中dROM値 (酸化ダメージの指標値)